2025年10月16日、弊社CEO 森英一朗、弊社科学顧問の先生方(齋尾智英(徳島大学
)、杉江和馬(奈良県立医科大学)、青木正志(東北大学)、杉山正明(京都大学)、
森正之(石川県立大学)敬称略)の共同研究チームの最新研究が国際科学誌「Nature
Communications」に論文公開されました。日本のアカデミアの多種多様な技術や専門性
を集結させることで、初めて実現した成果です。
この論文では、弊社の分子の動きを捉えるコア技術である「MAGmir(読み:マグミル、
*1)」により、神経変性疾患のひとつである筋萎縮性側索硬化症(以下、ALS、*2)
の病態発症メカニズムに、
「ジンクフィンガードメイン(ZnF)」という因子が重要な機能を持つことを明らかに
しました。
ALSは、運動神経が徐々に機能を失い、筋力低下や呼吸障害を引き起こす進行性の難
病であり、根本的な治療法の確立が課題となっています。
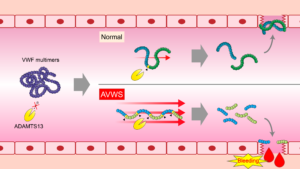
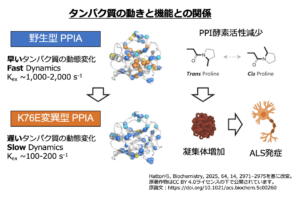
これまでの研究から、ALSなどの神経変性疾患では、タンパク質が細胞内でゆるやかに
結びついたり離れたりする「相分離」という現象に異常が起き、やがて塊(凝集体)を
形成して細胞の働きを妨げることが知られています。
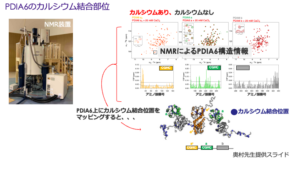
今回の研究では、ALS患者由来のiPS細胞を用いた解析を手掛かりに、ZnFという因子
の働きを解析しました。ZnFは古くから、DNA結合タンパク質として認識されていた因
子です。核磁気共鳴法(NMR)を含む、分子の様々な構造動態評価技術による詳細な
解析の結果、ZnFが凝集に繋がる状態のタンパク質を識別し、結合することで凝集を抑
えるという、新たな役割を持つことを発見しました。
この成果は、ZnFが正常に働けばALSは発症しない可能性があるという、発症の根本
に迫る新しい視点をもたらしました。ZnFそのものを薬にするには、様々な乗り越えな
ければいけない課題がまだまだ多くあります。しかしながら、今回明らかになったZnF
の機能を更に掘り下げて理解を深めていくことで、ALSの治療薬の糸口を見出し、その
過程でALS治療薬の種(シーズ)を生み出すことに繋がっていくと期待しています。
モルミルでは様々なアカデミアの最新知見を取り入れながら、患者様に希望を届ける
一歩となるよう創薬開発にこれからも取り組んでまいります。
詳しくは以下の記事をご覧ください。
▼日本経済新聞「奈良県立医科大学など、ALS原因抑制の因子発見 治療法開発に期待」
https://www.nikkei.com/article/DGXZQOUF16AG80W5A011C2000000/
▼奈良テレビNEWS「県立医大などの研究チーム ALSの原因を抑制する因子を発見」
https://www.naratv.co.jp/tvnnews/detail.html?id=394d41536175612b7051656b2b33466a335162
6542413d3d
▼奈良テレビNEWS (YouTube)「県立医大などの研究チーム ALSの原因を抑制する因子を発見
▼ANNnewsCH (YouTube)「難病ALSの原因物質を抑制する因子発見 治療法の開発につながると
期待【知っておきたい!】【グッド!モーニング】(2025年10月22日)」
論文本文はこちら:
「Zinc finger domains bind low-complexity domain polymers」
https://www.nature.com/articles/s41467-025-64382-2
(1):MAGmir 核磁気共鳴法(3)を利用した詳細な分子動態情報を取得する方法
(2) :筋萎縮性側索硬化症(ALS) 筋肉が萎縮し、力が弱くなっていく病気。筋肉そのものではなく、筋肉を動か し、運動をつかさどる神経(運動ニューロン)が障害を受ける。これにより筋 肉を動かす命令が伝わらなくなることで、筋肉が痩せていく。
(3):核磁気共鳴法(NMR)
NMRはNuclear Magnetic Resonanceの略。磁場中に置いた物質の原子核が自転し、電磁波に応答する性質を利用して、分子の構造や性質、運動状態を調べる分析手法。溶液中における生体分子を原子分解能で観察することができる。


-300x160.jpeg)